例1比较Fe2O3、FeO、Fe3O4中氧元素质量分数的大小。
基本解题思路
Fe2O3中氧元素质量分数大小=
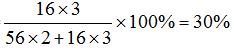
FeO中氧元素质量分数大小=
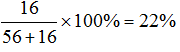
Fe3O4中氧元素质量分数大小=
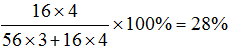
解题技巧分析
比较氧元素质量分数的大小实质上是比较三个分数的大小,小学数学的比较分数大小的两条基本思路一是分子相同,分母大的反而小;二是分母相同,分子大的大。由于三个分子中都含有16,因此可变形为:
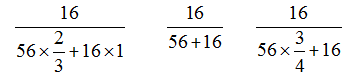
分母中都有16和56,因此只观察分母中的分数2/3. 3/4即可。1> 3/4>2/3,
因此可得三个质量分数大小关系为Fe2O3 >Fe3O4 >FeO
实战技巧
Fe2O3、FeO、Fe3O4变形为:
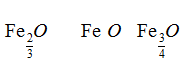
比较铁原子“个数”可快速得出答案。
河南真题:
相同质量的磷、铁、镁分别在氧气中完全燃烧,消耗氧气最多的是_____。
基本解题思路
等质量三个化学方程式有关的计算题
解题技巧分析
由于三种物质在氧气中燃烧产物分别为P2O5、Fe3O4 、MgO,因此问消耗氧气多少实质是问三种氧化物中氧元素的多少。
问题转换:由于题目中是相同质量的磷、铁、镁,它们的相对原子质量分别为31、56、24,转化为相等数据运算量太大,因此把问题转化为:若三种氧化物中氧元素相等,则磷、铁、镁三种元素质量大小关系为:
实战技巧
若三种氧化物中氧元素相等,则磷、铁、镁三种元素质量大小关系为:
P2O5、Fe3O4 、MgO变形为:

由结果可知,需要磷铁镁的大小关系为:磷<镁<铁
转化为原命题可知消耗氧气的多少关系为磷>镁>铁
竞赛
已知MgS、NaHSO3、MgSO4中硫元素的质量分数为32%,则氧元素的质量分数为
A.24%B.44%C.16%D.32%
【分析】根据NaHS、MgSO4、NaHSO3的化学式,可以发现NaH相对原子质量和为24,可以看成与Mg是等同的;即可以把NaH它们看成一个整体,就可以通过硫的质量分数求镁的质量分数,余下的就是氧元素质量分数.
【解答】解:因为NaHS、NaHSO3组成中钠和氢的个数比是1:1,可以把钠元素和氢元素放在一起看做镁元素(23+1=24),这样三种物质相当于是MgS、MgSO4、MgSO3,此时三种物质中